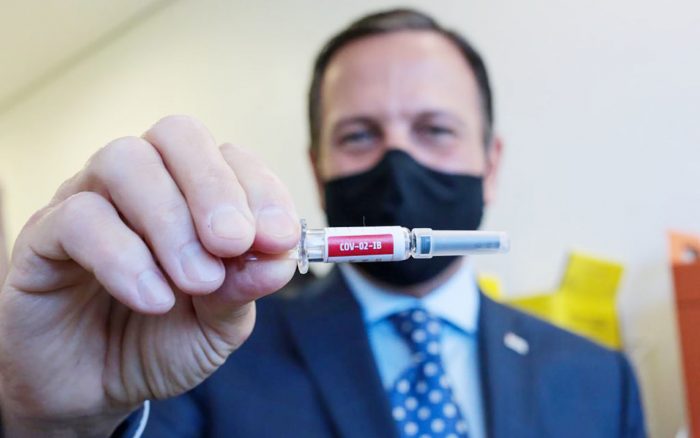
O governador João Doria (PSDB) afirmou nesta quarta-feira, 30 de setembro, que, se a CoronaVac passar na fase de testes em voluntários e for aprovada pela Agência Nacional de Vigilância Sanitária (Anvisa), a vacinação poderá ocorrer já a partir de 15 dezembro, começando por profissionais de saúde. Os testes seguem até 15 de outubro.
“Estamos confiantes no resultado dessa vacina. Estamos avançando positivamente com esperança de que essa será uma das mais promissoras vacinas contra a covid-19. Vamos respeitar os procedimentos de testagem, e após aprovação da Anvisa, o início da vacinação está previsto para começar no dia 15 de dezembro, começando pelos profissionais da saúde”, afirmou Doria.
O governador assinou o termo de compromisso com a biofarmacêutica Sinovac Life Science para fornecimento de 46 milhões de doses da CoronaVac ao estado de São Paulo até dezembro de 2020. O potencial imunizante contra o coronavírus é desenvolvido em parceria com o Instituto Butantan.
Doria também esclareceu que já há um entendimento verbal entre a direção do Butantan e a Sinovac para que outras 14 milhões de doses da vacina sejam fornecidas em fevereiro de 2021. O acordo foi assinado no Palácio dos Bandeirantes.
Além de Doria, assinaram o documento o diretor do Butantan, Diamas Tadeu Covas, e o vice-presidente mundial da Sinovac, Weining Meng. No valor de US$ 90 milhões, o contrato também formaliza a transferência de tecnologia para produção da vacina pelo instituto.
Até dezembro, a farmacêutica vai enviar seis milhões de doses da vacina já prontas, enquanto outras 40 milhões serão formuladas e envasadas em São Paulo. A segurança do imunizante já foi comprovada em uma pesquisa com mais de 50 mil voluntários na China.
Do total de voluntários, 94,7% não tiveram nenhuma reação adversa. Outros 5,36% sentiram efeitos adversos, todos de baixa gravidade, como dor no local da aplicação (3,08%), febre moderada (0,21%) e fadiga e perda de apetite (1,53%). Começaram na China os testes em crianças e idosos.
Entre as pessoas com mais de 60 anos, a vacina foi aplicada em 422 voluntários e os resultados apontaram 97% de eficácia. Os estudos em crianças têm 552 voluntários de 3 a 17 anos. No total, foram aplicadas 67.260 doses da CoronaVac em 50.027 pessoas, ação que foi autorizada pelo governo chinês para alguns grupos, como pacientes de risco e funcionários da Sinovac.
A vacina também já vem sendo testada no Brasil desde julho e, atualmente, os estudos clínicos da última fase são acompanhados por doze centros de pesquisa científica em cinco estados e no Distrito Federal. O Hospital das Clínicas da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (HCFMRP/ USP) participa dos testes da nova vacina.
O HC iniciou os testes da nova vacina contra o coronavírus em 30 de julho. Foram selecionados 500 voluntários para receber a vacina. No último dia 25, Doria anunciou a ampliação da testagem para mais quatro centros de pesquisa em Barretos (SP), Campo Grande (MS), Cuiabá (MT) e Pelotas (RS).
Com isso, a quantidade de voluntários do estudo coordenado pelo Instituto Butantan será ampliada de nove mil para 13 mil voluntários. O perfil dos voluntários que poderão se candidatar ao estudo permanece praticamente o mesmo. Profissionais da saúde que estejam trabalhando no atendimento a pacientes com covid-19.
Tanto na China como no Brasil, os testes clínicos passaram a envolver voluntários com mais de 60 anos, que são o grupo mais suscetível aos sintomas graves da covid-19. De acordo com o Butantan, que coordena a pesquisa no Brasil, a expectativa é que os testes de eficácia da CoronaVac sejam encerrados até o dia 15 de outubro.
Se o imunziante tiver sucesso na última etapa dos testes, o instituto pedirá a aprovação emergencial do imunizante à Anvisa. O objetivo do governo é iniciar uma campanha de vacinação contra o coronavírus na segunda quinzena de dezembro, com prioridade para profissionais de todas as unidades públicas e privadas de saúde de São Paulo.